判定基準:CTCAEのグレードの考え方
CTCAEは、有害事象の重症度をGrade 1(軽度)からGrade 5(死亡)まで標準化して評価する枠組みです。血液毒性は主にヘモグロビン(Hb)、好中球絶対数(ANC)、血小板数(Plt)、白血球数などの検査値の閾値に基づき定義され、臨床的所見(例:発熱の有無)を加味して重症度が決定されます。数値の基準は成人を前提としています。また、測定単位(例:/µLと×10^9/L)の整合を取ることに加え、施設ごとに異なる施設基準範囲との区別が必要です。表1に、代表的な血液毒性についてまとめました。具体的な数値閾値はCTCAE最新版1National Cancer Institute (NCI)、Division of Cancer Treatment and Diagnosis (DCTD), Cancer Therapy Evaluation Program (CTEP), “CTCAE and AE Reporting”、 NCI, 2025、https://dctd.cancer.gov/research/ctep-trials/for-sites/adverse-events、2025年9月6日 2Japanese Clinical Oncology Group (JCOG)、「CTCAE v5.0 日本語訳 JCOG 版」, JCOG、2022、https://jcog.jp/doctor/tool/ctcaev5/、2025年9月6日を参照ください。
| 毒性 | 評価指標 | 判定基準 | 備考 |
|---|---|---|---|
| 貧血 | ヘモグロビン(Hb) | Hb低下の度合いでグレード化 | – |
| 好中球減少 | 好中球絶対数(ANC) | ANCの閾値でグレード化 | 発熱の有無で発熱性好中球減少症(FN)として別扱い |
| 血小板減少 | 血小板数(Plt) | Plt低下の度合いでグレード化 | – |
電子カルテ由来DBで血液毒性を補足する方法
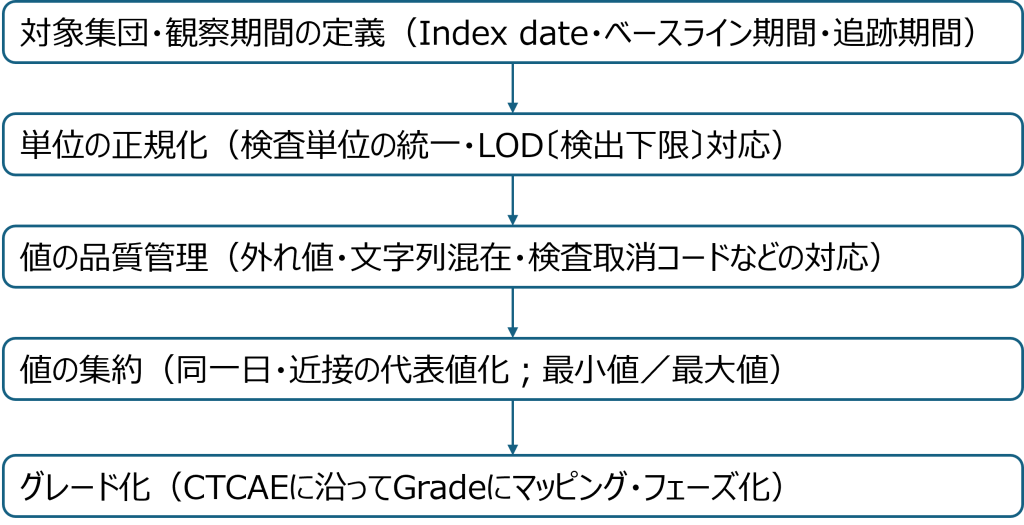
電子カルテ由来DBでは検査値を取得できるため、CTCAEに準拠した血液毒性評価を実臨床データで検討できます。そのうえで、解析時に気を付けるべきポイントは以下のとおりです。DBの検査値テーブル(検査項目コード、実測値、単位、検体採取日時/検査実施日時など)から、図1に示す手順で血液毒性のイベントを特定します。
- 対象集団・観察期間の定義:曝露と反応の前後関係を担保するため、治療レジメン投与開始日(index date)と、その前後のベースライン期間(例:-30日〜index dateの前日)および追跡期間(例:index date〜+180日)を定義する。
- 単位の正規化:施設・期間によらず一貫した基準で閾値の適用を可能にするため、ヘモグロビン(g/dL)、好中球数(/µLまたは×10^9/L)、血小板数(/µL)などの共通単位へ換算する。基準範囲の版や装置変更の影響にも留意し、検出下限(LOD)表記への対応をおこなう。
- 値の品質管理:測定誤差や入力ノイズによる偽の異常を防ぐため、ルールに基づく外れ値の除外(生理学的に非現実的な値など)、文字列混在・検査取消コードなどへの対応をおこなう。
- 値の集約:同一日・近接時間の重複測定は臨床的に妥当な代表値へ集約する。値の低下が毒性判定の規準となる項目(Hb、ANC、Plt)では「最小値」を採用、上昇が基準となる項目では「最大値」など、指標に応じた集約規則をあらかじめ定義しておく。
- グレード化: CTCAEの閾値に沿って値をGradeにマッピング。必要に応じて連続する複数の各採血点をまとめることで、「初回発生日」「最高Grade」「持続日数」「反復回数」なども把握可能。
- 1National Cancer Institute (NCI)、Division of Cancer Treatment and Diagnosis (DCTD), Cancer Therapy Evaluation Program (CTEP), “CTCAE and AE Reporting”、 NCI, 2025、https://dctd.cancer.gov/research/ctep-trials/for-sites/adverse-events、2025年9月6日
- 2Japanese Clinical Oncology Group (JCOG)、「CTCAE v5.0 日本語訳 JCOG 版」, JCOG、2022、https://jcog.jp/doctor/tool/ctcaev5/、2025年9月6日
この記事はメール会員専用の記事です。
メール会員登録すると続きをお読みいただけます。